Успехи и деятельность терапии CAR-T в медицинском центре Шиба, Израиль – 2024
Представляем ключевые моменты из лекции доктора Авигдора Авраама, директора Института гематологии и сопредседателя отделения гематологии и трансплантации костного мозга в медицинском центре Шиба. Эта лекция была представлена на конференции EBMT, которая проходила в феврале 2024 года в Севилье, Испания. (Для подробностей вы можете ознакомиться с записью выступления, начиная с отметки 21:20.)

Сегодня я хотел бы поделиться нашим опытом применения терапии CAR-T клетками по принципу "point-of-care" на достаточно большой группе пациентов в одном медицинском центре. Во многих странах доступность этой терапии ограничена из-за таких факторов, как сложности производства, региональные барьеры, нехватка квалифицированного персонала и проблемы с возмещением затрат. Еще одной серьезной проблемой одобренных препаратов является длительный процесс их производства, что представляет значительную угрозу для пациентов с быстро прогрессирующими заболеваниями.

В настоящее время три коммерческих продукта CAR-T клеток, нацеленных на CD19, одобрены Министерством здравоохранения Израиля. Однако коммерческий продукт CAR-T клеток, нацеленных на BCMA, пока не получил одобрения в стране.
Кроме того, в Израиле проводится три академических клинических исследования, два из которых включают CAR-T клетки, нацеленные на CD19 и BCMA, производимые локально в медицинском центре Шиба.
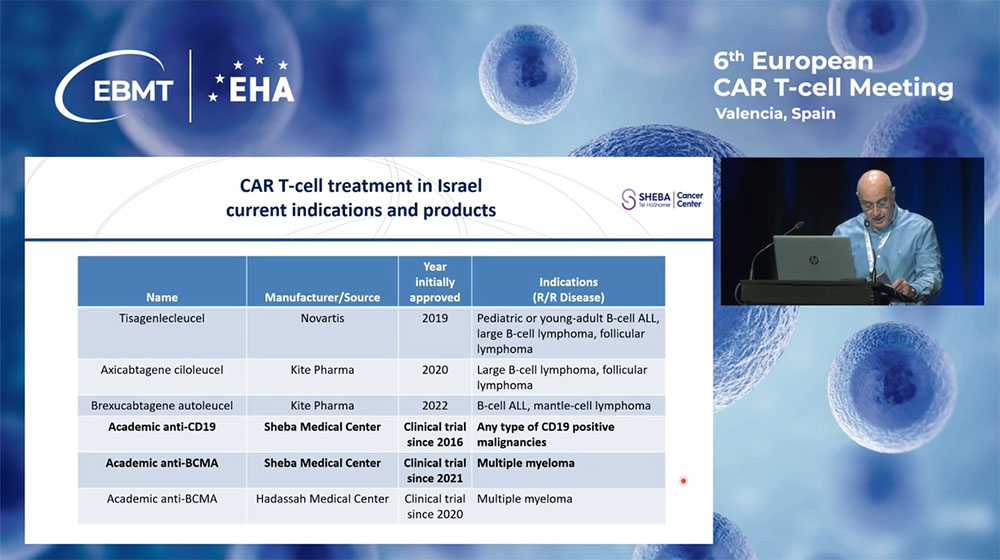
В 2016 году, за три года до появления первого коммерческого продукта в Израиле, мы начали производство CAR-T клеток, нацеленных на CD19, в рамках клинических испытаний фаз 1b и 2 для лечения различных гематологических заболеваний.
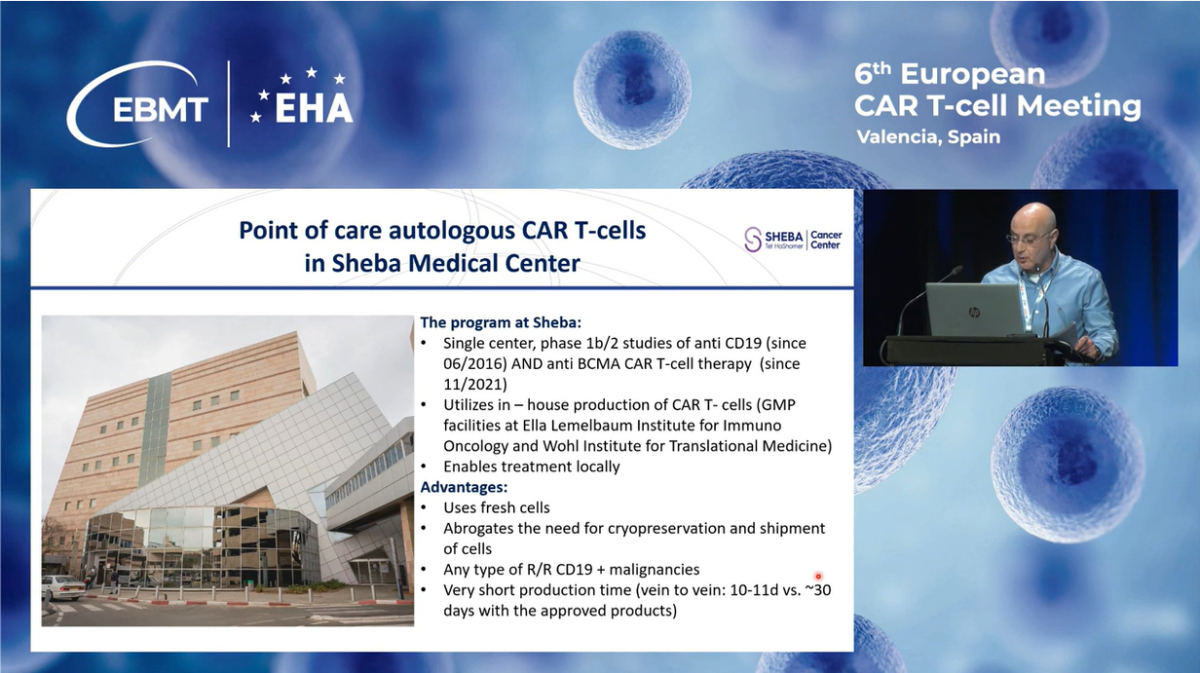
С ноября 2021 года мы расширили нашу программу, добавив терапию CAR-T клетками, нацеленными на BCMA. Эти клетки производятся вручную в GMP-лабораториях медицинского центра Шиба.
Локальное производство имеет ряд преимуществ: использование свежих клеток исключает необходимость их криоконсервации и транспортировки, снижает стоимость лечения и, что особенно важно, сокращает время "от вены до вены" до всего 10–11 дней. Наша программа позволяет оказывать помощь практически любому пациенту с CD19-положительными злокачественными заболеваниями, включая тех, для кого другие варианты лечения недоступны.
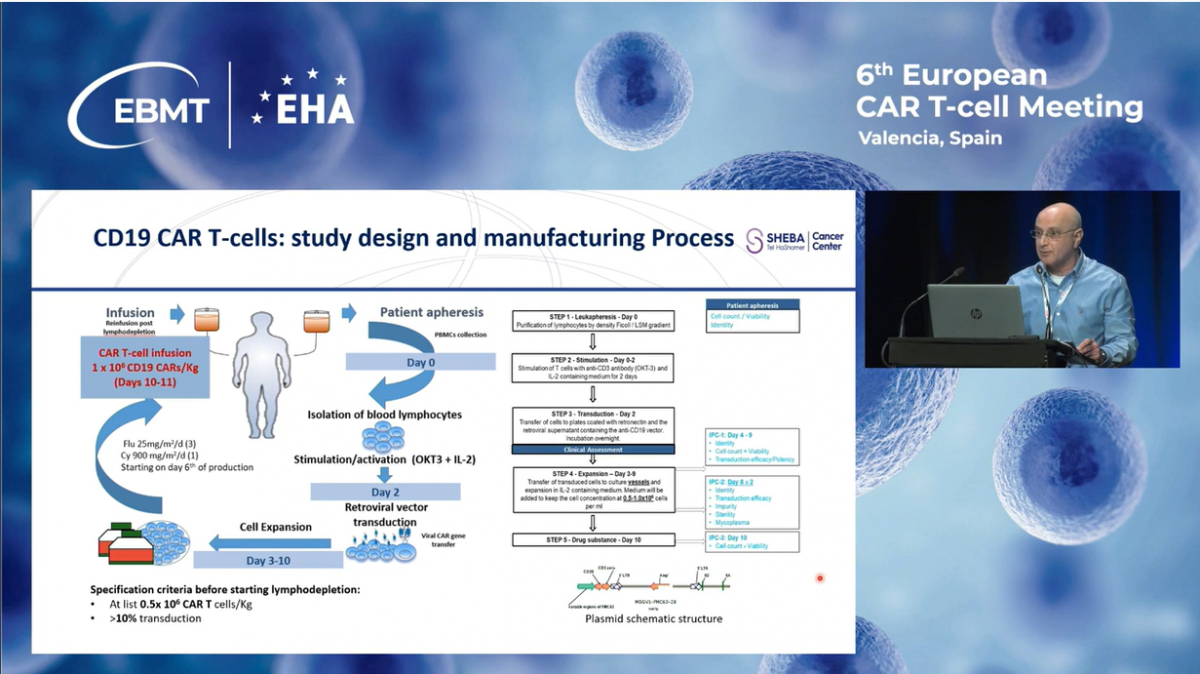
Основными критериями участия в нашей программе являются наличие злокачественных опухолей, экспрессирующих CD19. Кандидатами могут стать пациенты, у которых заболевание оказалось устойчивым к стандартной терапии или произошло рецидивирование после лечения, включая рецидивы после трансплантации.

Основными целями этого исследования были оценка безопасности и общего уровня ответа через 28 дней после введения CAR-T клеток. Второстепенные цели включали общую выживаемость и выживаемость без прогрессирования заболевания.
Кроме того, возможность быстрой подготовки клеток позволяет нам предоставлять спасительную терапию пациентам, для которых отсутствуют подходящие коммерческие продукты.
Мы опубликовали наш опыт применения Т-клеточных продуктов после лейкафереза в условиях реальной клинической практики.
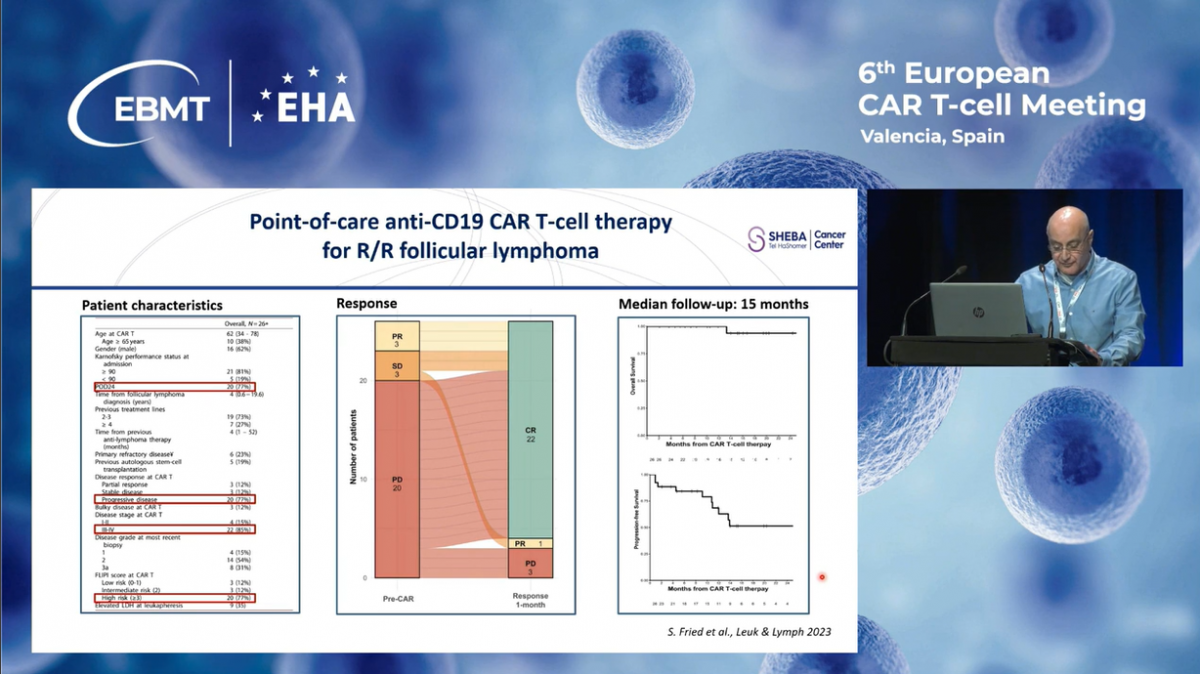
Этот слайд демонстрирует наш опыт использования терапии CD19 CAR-T по принципу "Point of Care" в медицинском центре Шиба.

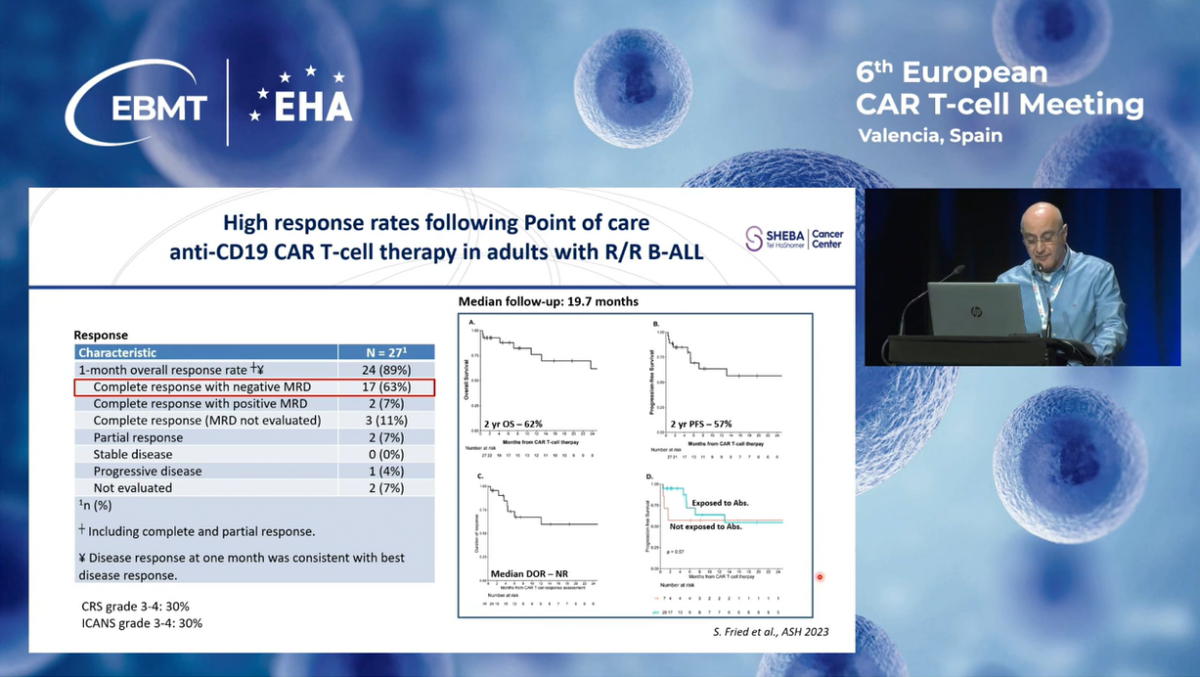
К январю 2024 года в программу были включены 321 пациент с рецидивирующими или рефрактерными CD19-положительными заболеваниями, среди которых 248 взрослых и 73 ребенка. Из всей группы 21 пациент не получил инфузию: у 17 из них это произошло из-за клинического ухудшения или быстрого прогрессирования заболевания, и только у 4 — по причине сбоев в процессе производства.

CAR-T для лечения множественной миеломы
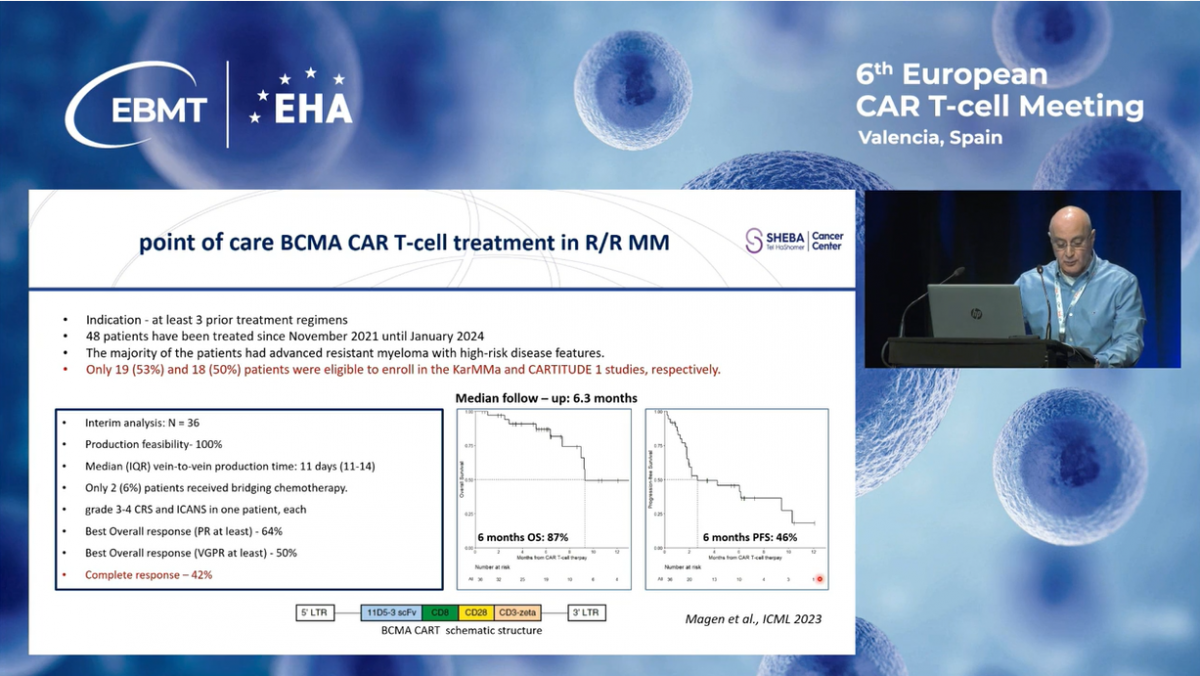
Хочу представить вам наши предварительные результаты лечения множественной миеломы с использованием локально произведенных BCMA CAR-T клеток.
С ноября 2021 года мы расширили программу, добавив терапию anti-BCMA CAR-T для пациентов с рецидивирующей или рефрактерной миеломой, которые прошли как минимум три линии лечения. Процесс производства идентичен тому, что применяется для CD19 CAR-T клеток. После 10-дневного культивирования пациенты получают девять миллионов свежих CAR-T клеток на килограмм массы тела.
К январю 2024 года в программу были включены 48 пациентов. Промежуточный анализ данных первых 36 пациентов показал общий уровень ответа в 64%, при этом полная ремиссия была достигнута у 45% пациентов.
Сводка программы CAR-T в медицинском центре Шиба
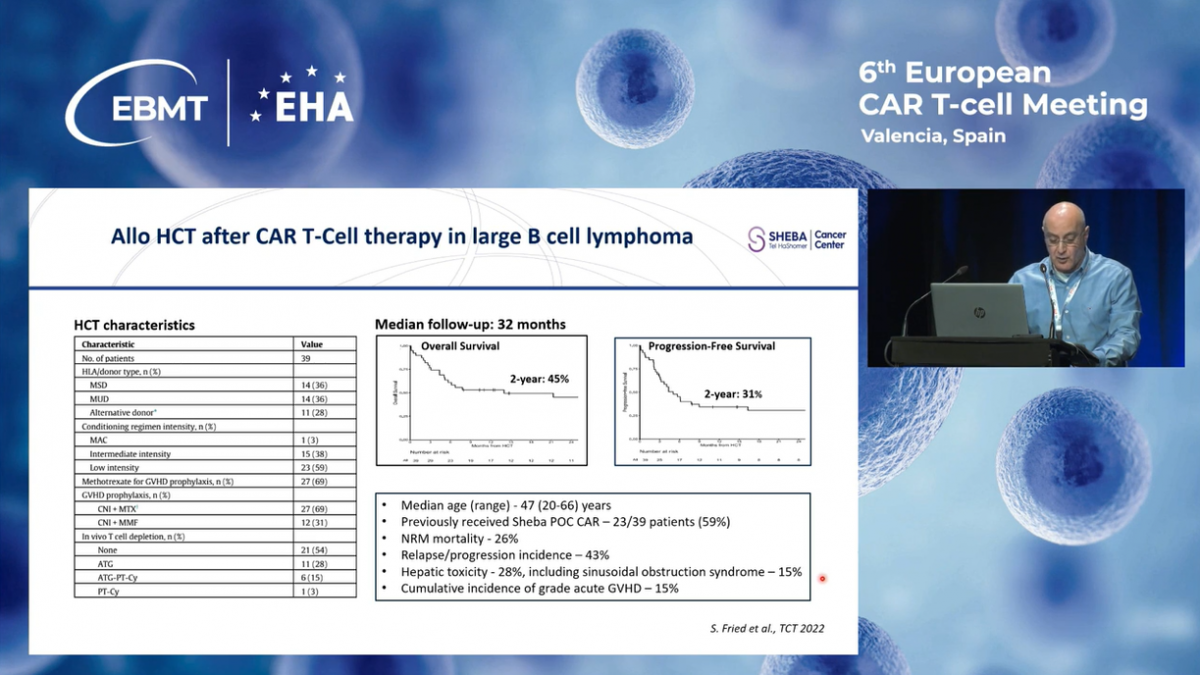
В завершение своей презентации хочу подчеркнуть, что лечение пациентов с рецидивирующей или рефрактерной крупноклеточной B-клеточной лимфомой, фолликулярной лимфомой и В-ALL с использованием локально произведенных CD19 CAR-T клеток демонстрирует хорошую переносимость, а долгосрочные результаты сопоставимы с достижениями коммерческих препаратов.
Наш опыт применения anti-BCMA CAR-T клеток по принципу "point-of-care" показывает высокие показатели ответа, обнадеживающие результаты выживаемости и отличный профиль безопасности при лечении рецидивирующей или рефрактерной множественной миеломы.
Локальное производство "point-of-care" отличается оперативностью и эффективностью. Оно исключает необходимость криоконсервации клеток и их транспортировки. Короткое время "от вены до вены" минимизирует потребность в поддерживающей терапии и снижает токсичность лечения для большинства пациентов.
Кроме того, в ближайшие месяцы планируется запуск новой программы "point-of-care", которая будет использовать полностью автоматизированную систему Cocoon для производства клеток.

Информация о CAR-T:














